2024 / 11 / 22 星期五
上報 Up Media
toggle- 最新消息 謝宜容起碼幹掉賴清德半壁江山 2024-11-22 00:02
- 最新消息 投書:立院惡鬥 只會讓更多科技人企業人不敢投身政壇 2024-11-22 00:00
- 最新消息 勞動部稱謝宜容失聯明天不出面 吳母淚控:霸凌太過分、太惡毒 2024-11-21 22:05
- 最新消息 俄烏戰況恐升級 烏克蘭是否有能力攔截ICBM 2024-11-21 21:50
- 最新消息 明後兩天各地氣溫回升 北部、東北部18到23度濕涼舒爽 2024-11-21 21:45
- 最新消息 劍橋詞典2024年度代表字出爐 「manifest」反映人們追求身心健康趨勢 2024-11-21 21:43
- 最新消息 為了9萬元勒斃馬國女大生 陳柏諺一審判賠父母逾638萬元 2024-11-21 21:32
- 最新消息 觸犯戰爭罪、違反人道法 ICC對納坦雅胡、哈瑪斯領導層發出逮捕令 2024-11-21 20:47
- 最新消息 【世棒四強賽】「CT AMAZE」自費飛東京應援 推掉台灣活動損失近10萬 2024-11-21 20:45
- 最新消息 蔡英文抵達加拿大 感謝台灣鄉親熱情接機 2024-11-21 20:37
【市占100%】胰膽藥「可使保朗」膠囊溶離度NG 5批號急回收
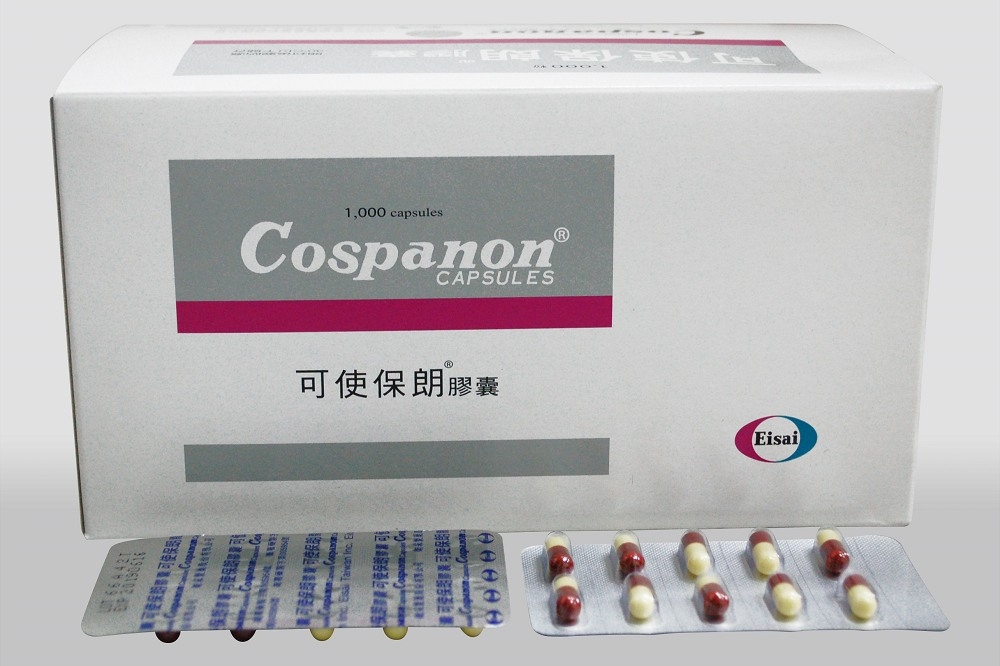
專治膽道疾病或胰臟炎痙攣的「可使保朗膠囊」溶離度不合格,估須回收120萬粒。(取自衛采製藥官網)
食藥署今天(9日)公布藥品回收警訊,市占率高達100%用於治療膽道疾病或胰臟炎引起的痙攣性症狀的「可使保朗膠囊」,因持續性安定性試驗之溶離度不合格,宣布回收5批號、約120萬粒膠囊。對此,食藥署藥品組科長洪國登表示,雖然同成分同劑型藥品只有這一款,但有新批號產品及不同成分用藥,民眾不用太過擔心。
由衛采製藥股份有限公司研發的「可使保朗膠囊(Cospanon capsules)」,廠商主動通報,部分批號藥品於持續性安定性試驗之溶離度結果未能符合規格,故啟動回收98A08T、98B09T、98C09T、98B08T、98A09T共5批藥,總數約120萬粒。
據了解,這款藥主要成分為Flopropione,用於緩解膽道疾病(膽石症、膽囊炎、膽管炎、膽割除後遺症等)所引起的痙攣性症狀、緩解胰臟炎所引起的痙攣性症狀。
(熱門點閱:把握這周好天氣! 濕冷鋒面下周襲台)
洪國登表示,這款藥是膠囊狀,藥品吞下肚進入腸胃道,膠囊外殼必須溶離才能溶出藥品,這次是廠商主動通報,在進行2年安定性試驗時發現,溶離度結果低於標準,顯示藥品的效果較差,因此啟動回收,廠商目前還在了解原因;由於該款藥品效期為3年,在效期內就低於標準,必須啟動回收。
洪國登指出,這款藥品健保申報用量每年約180萬粒,且同成分同劑型藥品只有這一款,市占率為百分之百,但有新批號產品,加上其他成分藥品可供選擇,患者不致於缺藥。他並提醒民眾,若對用藥有疑慮,應盡速回診與醫師討論,處方其他適當藥品。
食藥署已要求於3月24日前完成回收作業,並請請各醫療院所、藥商、藥局配合辦理回收作業,立即停止調劑、供應,同時要求衛采製藥應繳交回收成果報告書及後續預防矯正措施。
熱門影音
熱門新聞
- 【懶人包】勞動部公務員疑遭職場霸凌輕生 事件始末「時間軸、手段、調查結果」一次看懂
- 起底謝宜容!傳身家背景雄厚「善做公關」 先生和綠營高層有交情
- 一元特典!YOASOBI「超現實」小巨蛋演唱會釋出「零星票券」,11/24 採實名制一般販售
- 【世界棒球12強賽】滿足「2條件」台灣確定晉級4強 今晚是關鍵
- 先搶先贏!Ado 五月林口體育館演唱會採實名制入場,11/19 輸入「指定代碼」可優先預購
- 【內幕】T112步槍裝彈器採購案疑專利侵權 以色列向軍備局寄存證信函
- 王一博金雞獎典禮被抓包視線離不開趙麗穎 網揭兩人4年戀情無法曝光背後真相
- 勞動部涉職場霸凌不只謝宜容? 何佩珊:與輕生者中間還有2個主管











