2024 / 11 / 22 星期五
上報 Up Media
toggle- 最新消息 【有片】普丁證實用最新「榛果樹」飛彈攻擊烏國 具MIRV技術可攜多枚彈頭 2024-11-22 07:50
- 最新消息 陳嘉宏專欄:「勞動部慘案」的背後是賴政府失能 2024-11-22 07:02
- 最新消息 2024 高雄城市咖啡節週末登場!集結 60 家咖啡與甜點店 冰滴、手沖、咖啡酒通通有 2024-11-22 07:00
- 最新消息 投書:當APEC的C位不是美國而是中國 2024-11-22 07:00
- 最新消息 投書:藍白已是不分青紅皂白踐踏台灣民主法治 2024-11-22 07:00
- 最新消息 謝宜容起碼幹掉賴清德半壁江山 2024-11-22 00:02
- 最新消息 投書:立院惡鬥 只會讓更多科技人企業人不敢投身政壇 2024-11-22 00:00
- 最新消息 勞動部稱謝宜容失聯明天不出面 吳母淚控:霸凌太過分、太惡毒 2024-11-21 22:05
- 最新消息 俄烏戰況恐升級 烏克蘭是否有能力攔截ICBM 2024-11-21 21:50
- 最新消息 明後兩天各地氣溫回升 北部、東北部18到23度濕涼舒爽 2024-11-21 21:45
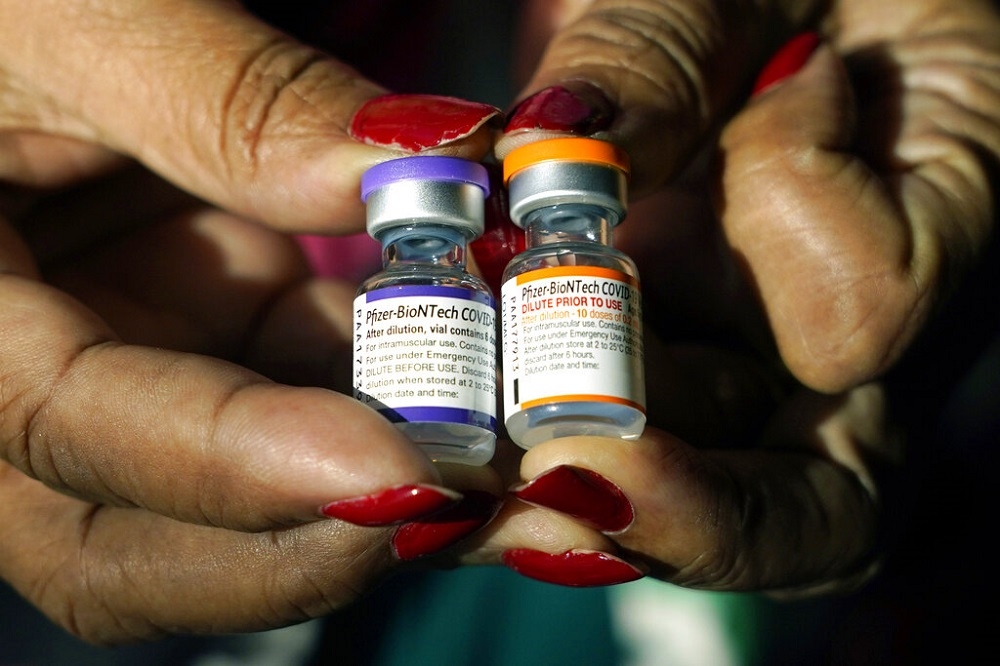
美國FDA於17日通過緊急使用授權,批准輝瑞疫苗的第三劑提供給5到11歲孩童接種。(美聯社)
美國食品藥物管理局17日通過緊急使用授權,批准輝瑞疫苗的追加劑用於5至11歲的孩童身上。接下來美國疾病管制暨預防中心將於19日召開外部專家會議,再由疾管中心主任做出最終決定。
路透指出,目前美國5歲以下的幼兒尚未被納入接種新冠疫苗的範圍內。美國食藥局(FDA)局長克里夫(Robert Califf)表示,允許5到11歲群體施打追加劑,是希望提供持續的保護力;不過美國的家長態度如何,仍待觀察。據美國疾管中心(CDC)數據,該群體僅有28.8%已完整接種,比例是各年齡層中最低。
費城兒童醫院的小兒傳染病專家奧菲特(Paul Offit)認為,開放該年齡層施打追加劑,對整體疫情的影響有限。他質疑追加劑的目標到底是什麼,「是希望抵抗所有的有症狀感染嗎?還是只針對重症?」他指出,從目前的證據看來,兩劑疫苗已經足以預防重症。
據美國有線電視新聞網報導,輝瑞於4月底申請緊急使用授權。當時提交的數據顯示,5到11歲孩童接種第三劑之後,體內抗Omicron變種的抗體增加了36倍。
根據紐約州衛生署和CDC的研究,在Omicron疫情期間,5到12歲孩童即使打過兩劑輝瑞疫苗,整體保護力仍從68%大幅降為12%;但針對重症和住院,還是能有效防護。
熱門影音
熱門新聞
- 【懶人包】勞動部公務員疑遭職場霸凌輕生 事件始末「時間軸、手段、調查結果」一次看懂
- 起底謝宜容!傳身家背景雄厚「善做公關」 先生和綠營高層有交情
- 一元特典!YOASOBI「超現實」小巨蛋演唱會釋出「零星票券」,11/24 採實名制一般販售
- 【世界棒球12強賽】滿足「2條件」台灣確定晉級4強 今晚是關鍵
- 先搶先贏!Ado 五月林口體育館演唱會採實名制入場,11/19 輸入「指定代碼」可優先預購
- 【內幕】T112步槍裝彈器採購案疑專利侵權 以色列向軍備局寄存證信函
- 王一博金雞獎典禮被抓包視線離不開趙麗穎 網揭兩人4年戀情無法曝光背後真相
- 勞動部涉職場霸凌不只謝宜容? 何佩珊:與輕生者中間還有2個主管











